T
Teach Me AnythingTMA
Video History
Page 25 / 47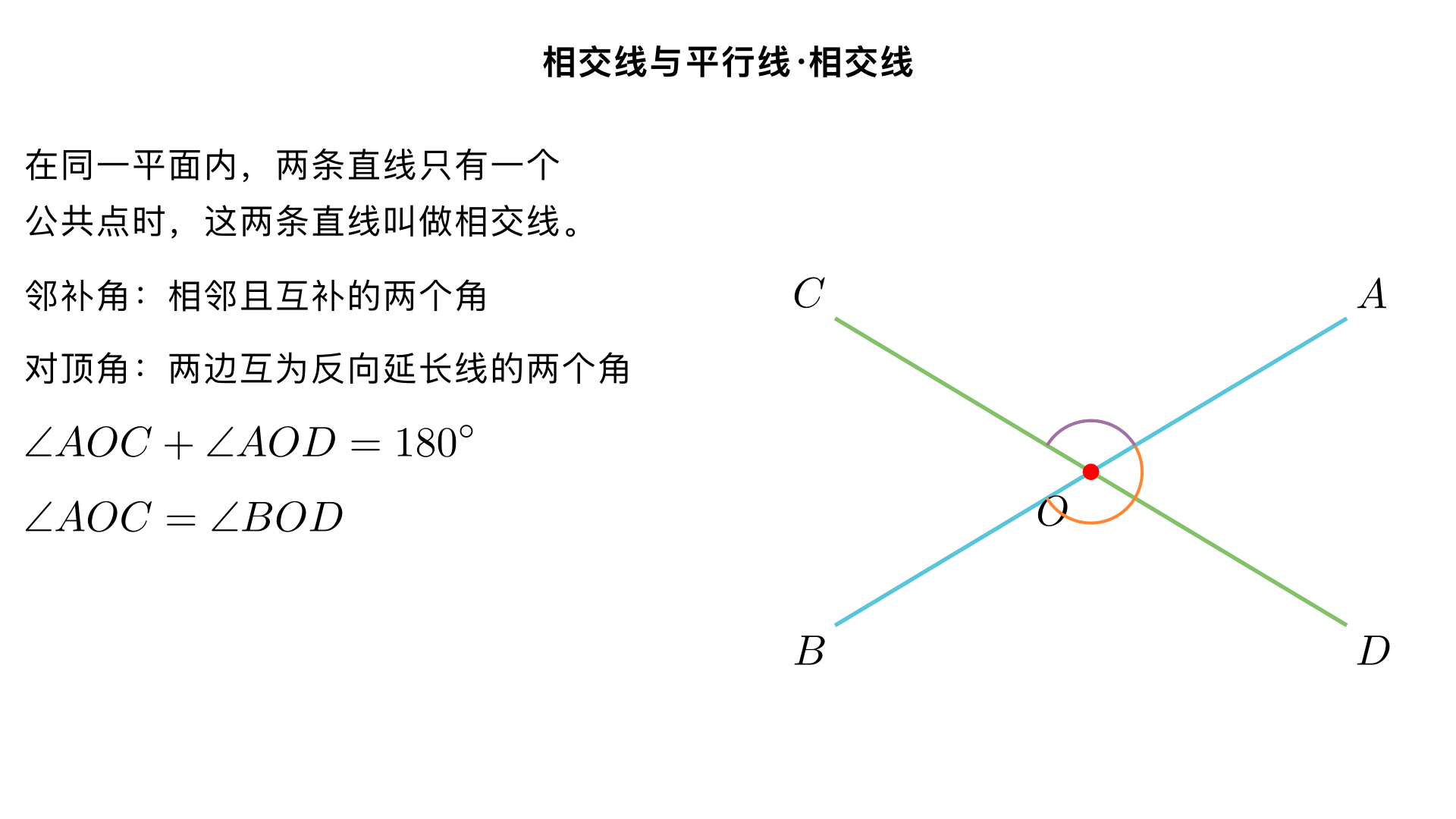
▶
七年级数学・相交线与平行线・相交线 一、相交线的基本概念 相交线的定义在同一平面内,两条直线只有一个公共点时,这两条直线叫做相交线,这个公共点叫做交点。例如:直线 AB 和直线 CD 相交于点 O,点 O 就是它们的交点。 邻补角 定义:两条直线相交时,相邻且互补的两个角叫做邻补角。 特征:① 有一条公共边;② 另一边互为反向延长线;③ 两个角的和为 180°。 示例:直线 AB 与 CD 相交于 O,∠AOC 和∠AOD 是邻补角,∠AOC+∠AOD=180°。 对顶角 定义:两条直线相交时,一个角的两边分别是另一个角两边的反向延长线,这两个角叫做对顶角。 特征:① 顶点相同;② 两边互为反向延长线;③ 对顶角相等。 示例:直线 AB 与 CD 相交于 O,∠AOC 和∠BOD 是对顶角,则∠AOC=∠BOD;∠AOD 和∠BOC 是对顶角,则∠AOD=∠BOC。 二、垂线 垂线的定义如果两条直线相交所成的四个角中有一个角是直角(90°),那么这两条直线互相垂直,其中一条直线叫做另一条直线的垂线,它们的交点叫做垂足。符号表示:若直线 AB⊥CD 于点 O,则∠AOC=90°。 垂线的性质 性质 1:在同一平面内,过一点有且只有一条直线与已知直线垂直。(“一点” 可以在直线上,也可以在直线外) 性质 2:连接直线外一点与直线上各点的所有线段中,垂线段最短,简称垂线段最短。 点到直线的距离从直线外一点到这条直线的垂线段的长度,叫做点到直线的距离。注意距离是 “长度”,是一个数值,而非线段本身。 三、相交线中的角度计算 核心依据 邻补角之和为 180°; 对顶角相等; 垂直的两条直线夹角为 90°。 典型例题已知直线 AB 和 CD 相交于点 O,OE⊥AB,∠EOD=65°,求∠AOC 的度数。解:∵OE⊥AB,∴∠AOE=90°∵∠AOE=∠AOD+∠EOD,∠EOD=65°∴∠AOD=90°-65°=25°又∵∠AOC 与∠AOD 是邻补角∴∠AOC=180°-25°=155°(或利用对顶角,若有其他条件也可灵活转换)
▶
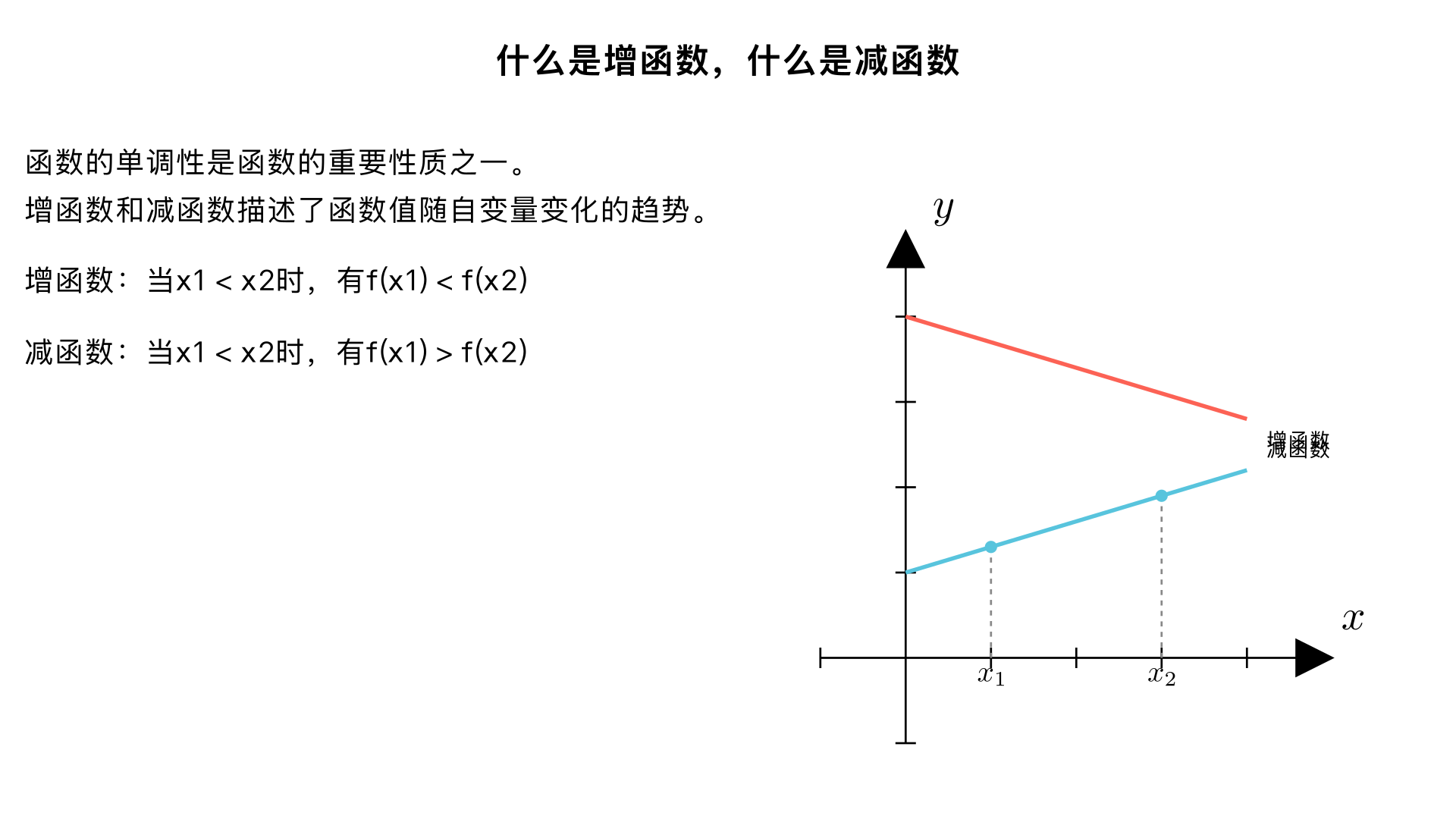
什么是增函数,什么是减函数
▶
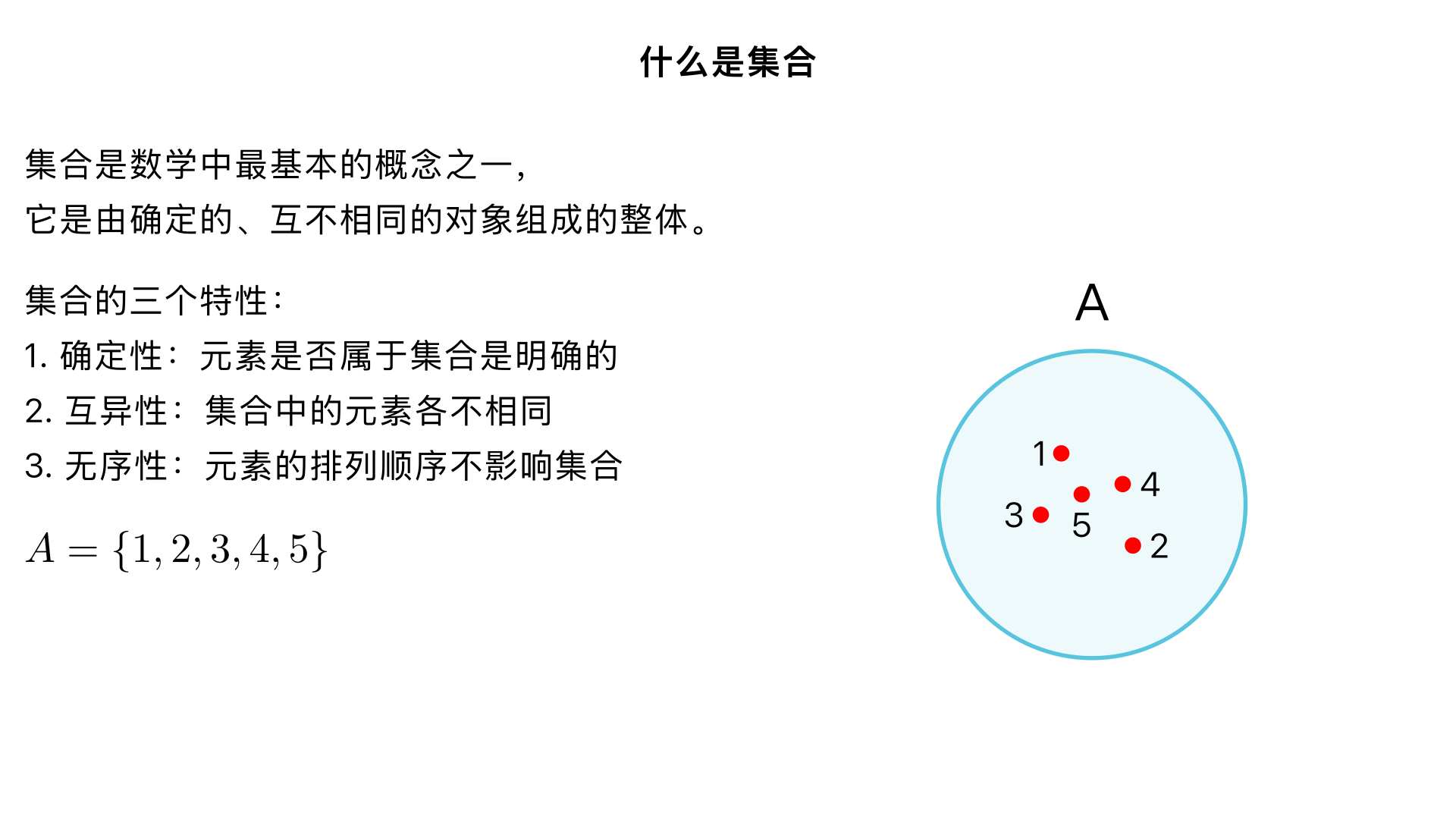
讲解什么是集合
▶
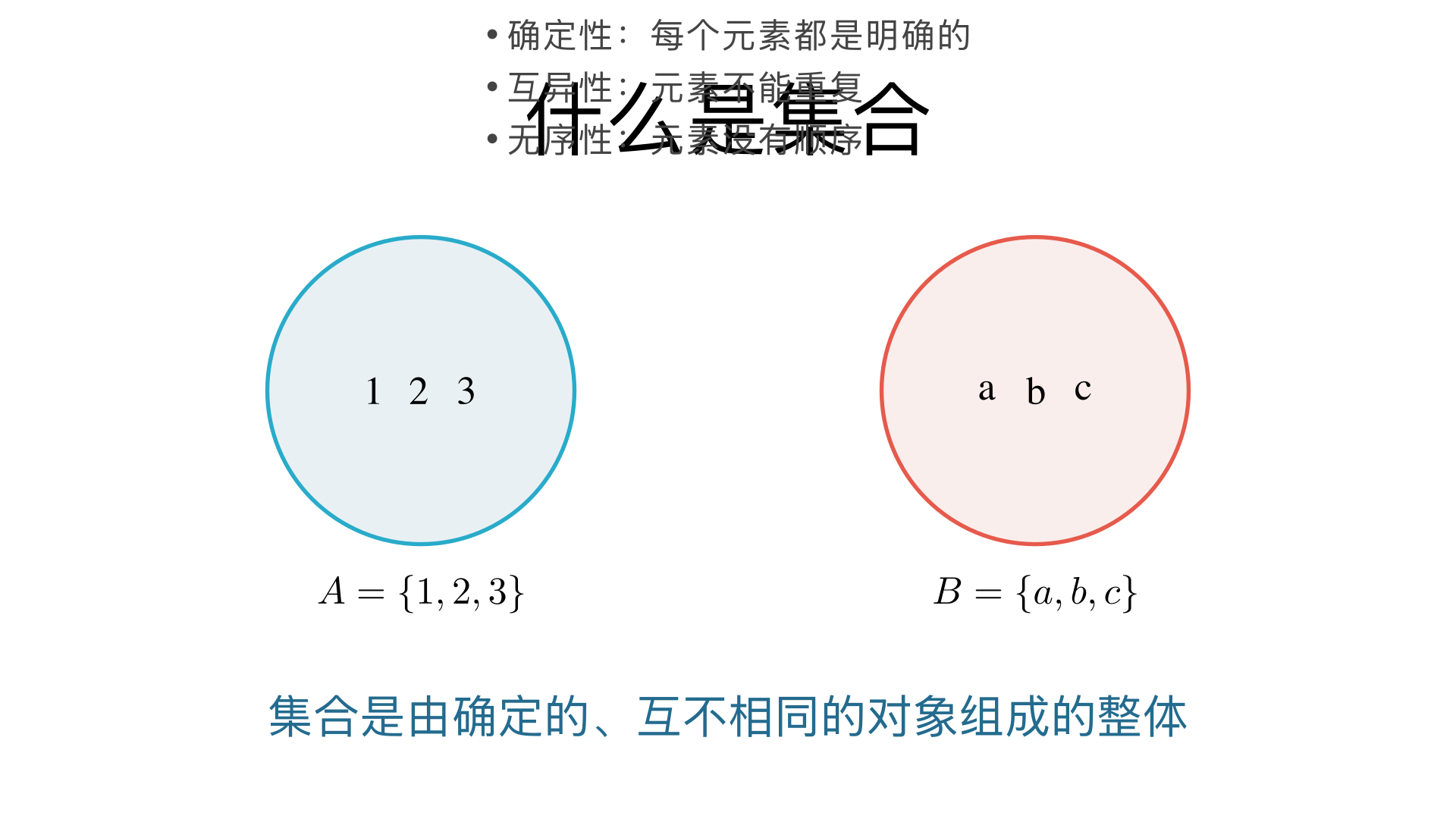
什么是集合
▶
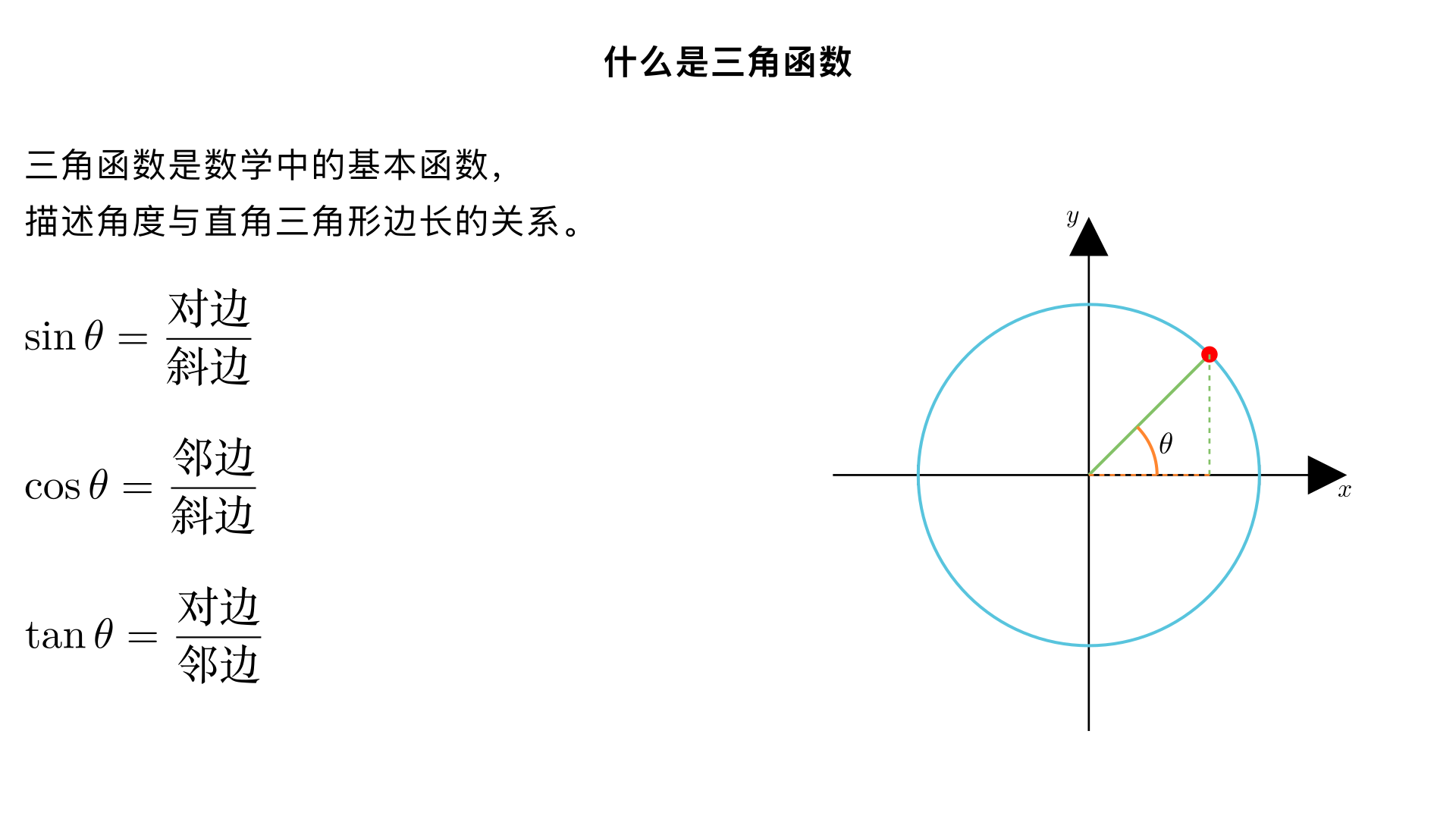
讲解 什么是三角函数
▶
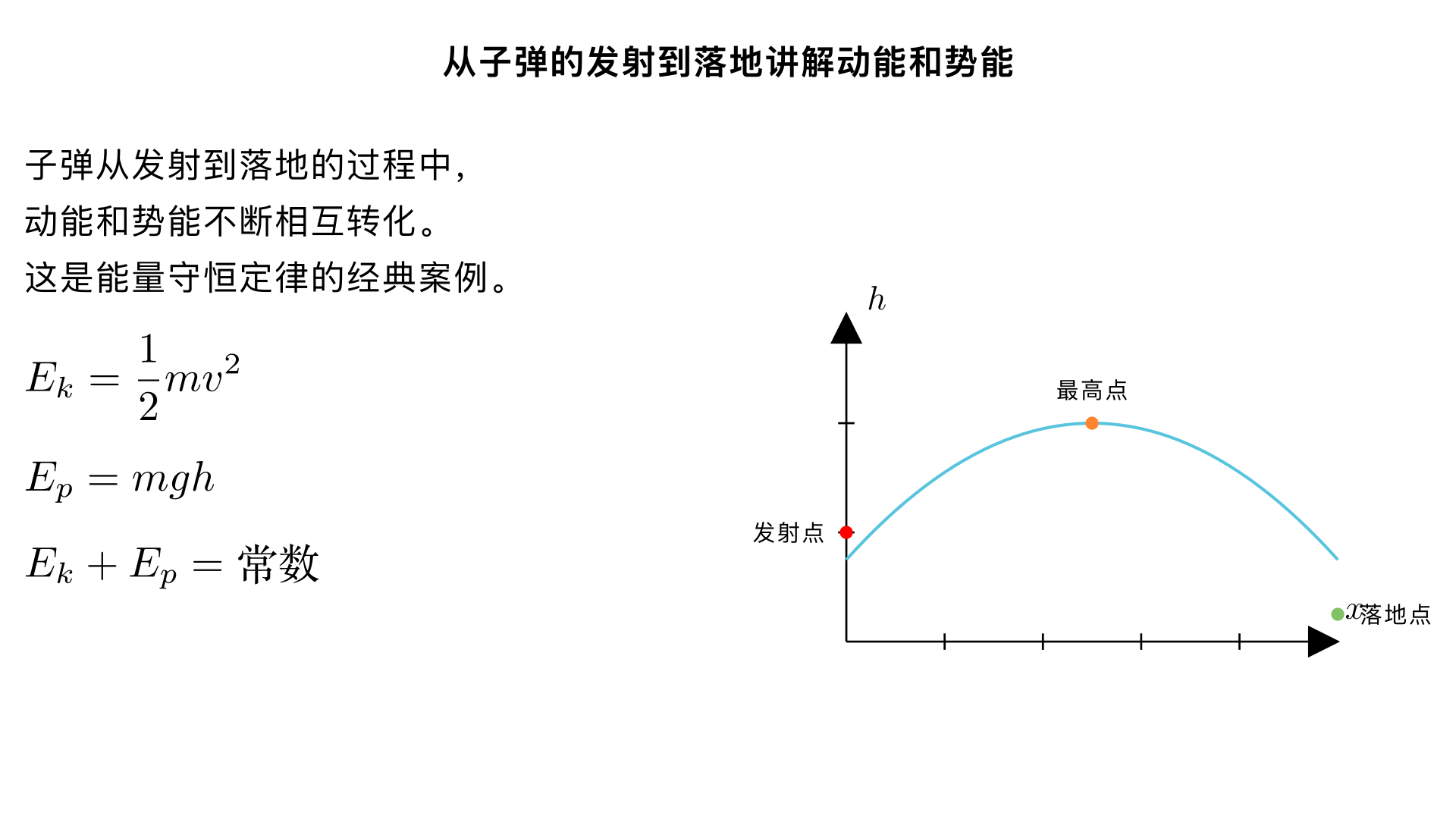
从子弹的发射到落地讲解动能和势能
▶
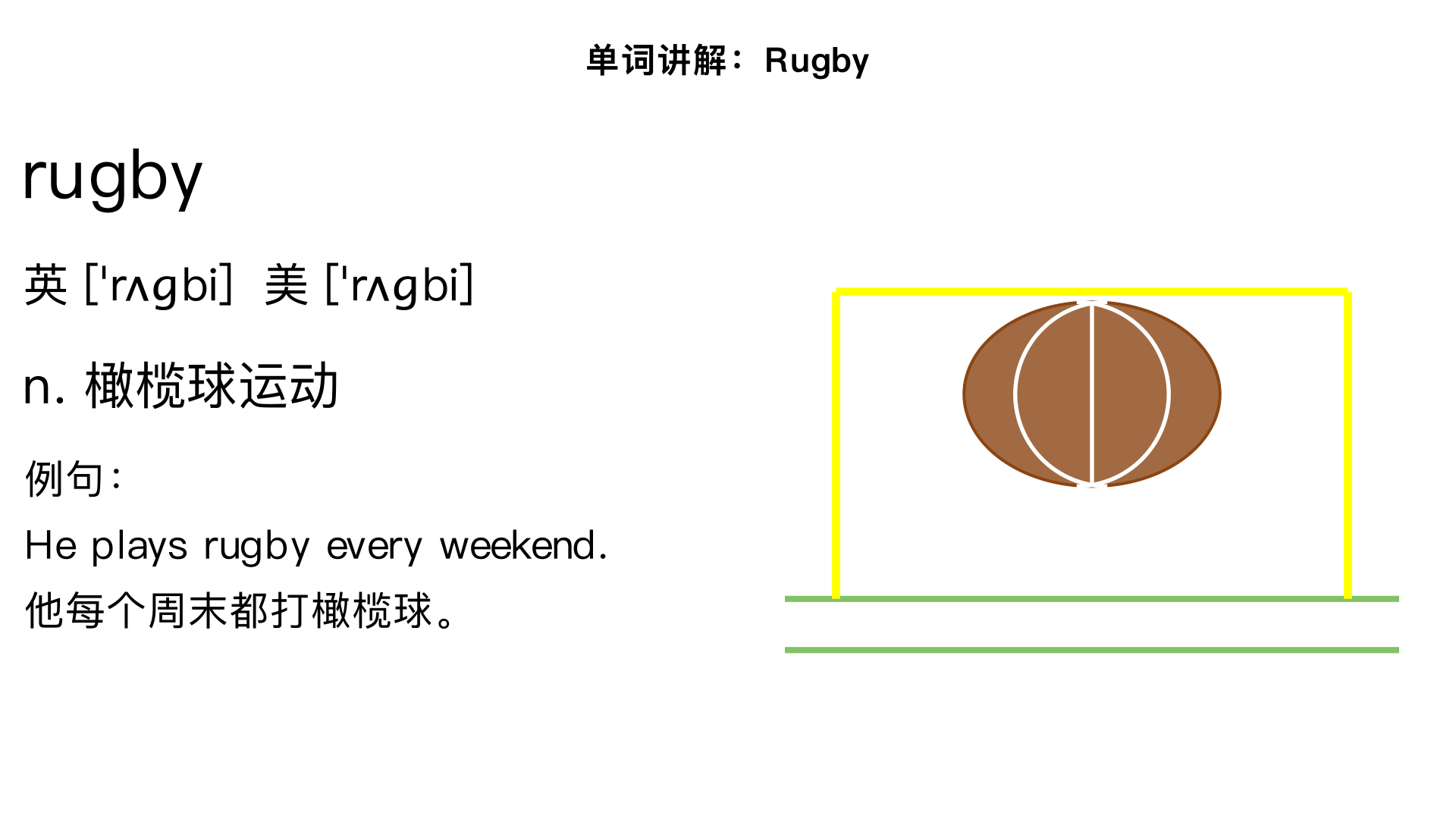
讲解单词 rugby

▶
讲解单词
▶
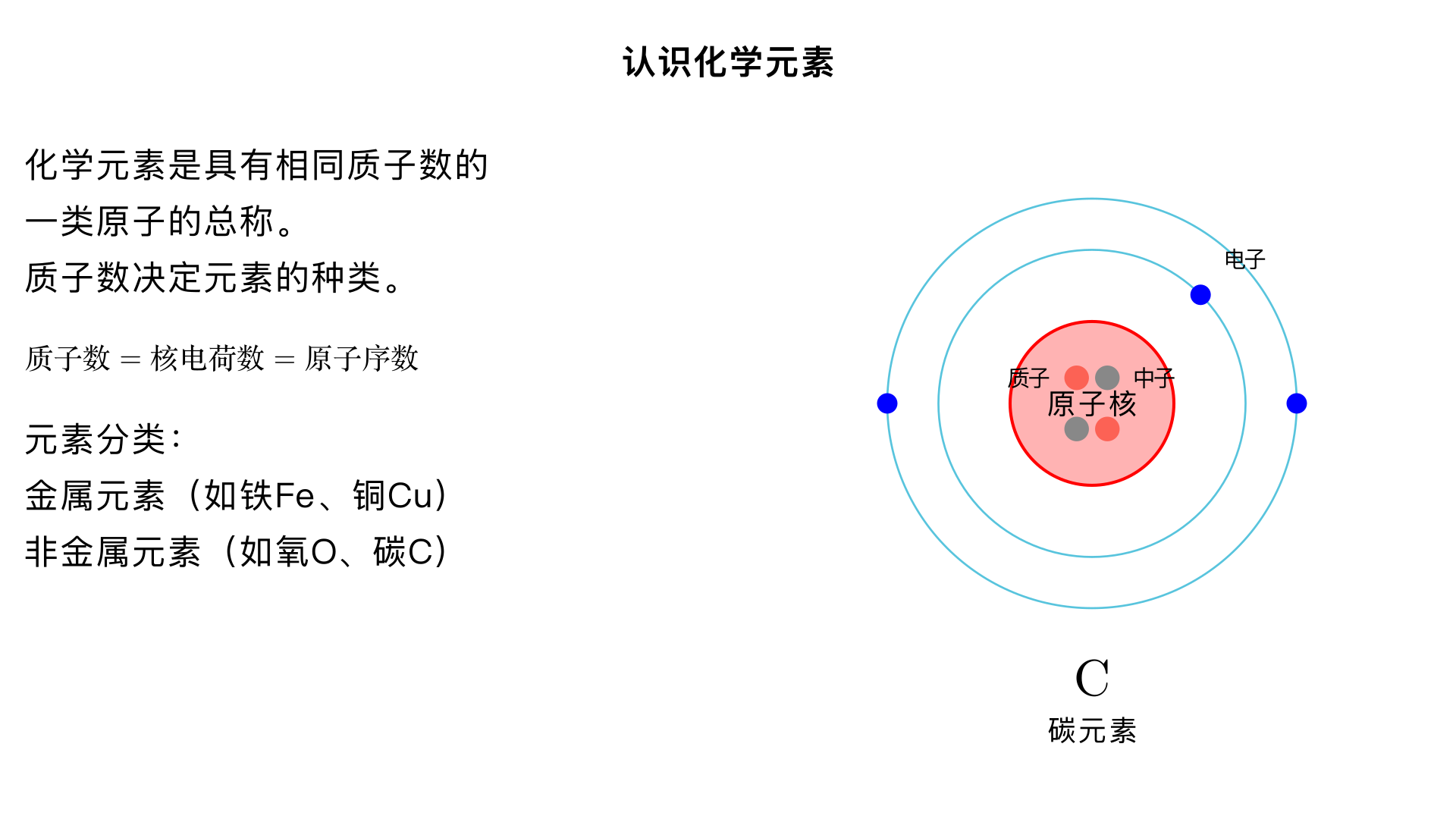
九年级化学・认识化学元素・化学元素 知识点梳理 一、化学元素的基本概念 定义 化学元素是具有相同 ** 质子数(即核电荷数)** 的一类原子的总称。 注意:质子数决定元素的种类,同种元素的原子质子数一定相同,而中子数、电子数可能不同(如碳 - 12、碳 - 13、碳 - 14,质子数均为 6,中子数分别为 6、7、8)。 元素与原子的区别与联系 | 对比维度 | 元素 | 原子 | | ---- | ---- | ---- | | 概念范畴 | 宏观概念,只讲种类,不讲个数 | 微观概念,既讲种类,又讲个数 | | 描述对象 | 物质的宏观组成(如氧气由氧元素组成) | 物质的微观构成(如一个氧分子由两个氧原子构成) | | 联系 | 元素是同一类原子的总称,原子是元素的基本单元 | 二、元素的分类 九年级阶段主要将元素分为金属元素、非金属元素(包括稀有气体元素)两大类: 金属元素 汉字特点:除汞(俗称水银,常温下为液态)外,均以 “钅” 为偏旁(如铁 Fe、铜 Cu、铝 Al)。 化学性质:多数具有良好的导电性、导热性、延展性,在化学反应中易失去电子。 非金属元素 汉字特点:以 “气”“石”“氵” 为偏旁(如氧 O、碳 C、溴 Br)。 化学性质:一般导电性较差,在化学反应中易得到电子;其中稀有气体元素(如氦 He、氖 Ne)化学性质极不活泼,又称 “惰性气体”。 三、元素符号 书写规则 由一个字母表示的元素符号,必须大写(如氢 H、氧 O)。 由两个字母表示的元素符号,第一个字母大写,第二个字母小写(如铁 Fe、钙 Ca,注意不能写成 FE 或 fE)。 意义 宏观意义:表示一种元素。 微观意义:表示这种元素的一个原子。 特殊情况:对于由原子直接构成的物质(金属、稀有气体、部分固态非金属),元素符号还能表示这种物质(如 Fe 可表示铁元素、一个铁原子、铁这种物质)。 四、元素周期表(基础认知) 基本结构 元素周期表共有7 个横行(称为周期),18 个纵列(称为族,其中 8、9、10 三个纵列合为一个族)。 每一格包含的信息:原子序数(= 质子数 = 核电荷数 = 核外电子数)、元素符号、元素名称、相对原子质量(如氢元素一格:原子序数 1,符号 H,名称氢,相对原子质量 1.008)。 排布规律 同一周期的元素,电子层数相同,从左到右质子数依次递增。 同一族的元素,最外层电子数相同,化学性质相似。 五、常见易错点 混淆 “元素” 和 “原子” 的描述,如不能说 “水由两个氢原子和一个氧原子组成”,正确表述为 “水由氢元素和氧元素组成”,或 “一个水分子由两个氢原子和一个氧原子构成”。 元素符号书写不规范,如将 “铜” 写成 “CU”、“锰” 写成 “mn”。 误认为质子数相同的粒子一定是同种元素(粒子包括分子、原子、离子等,如 H₂O 和 Ne 质子数均为 10,但不是同种元素)。
▶
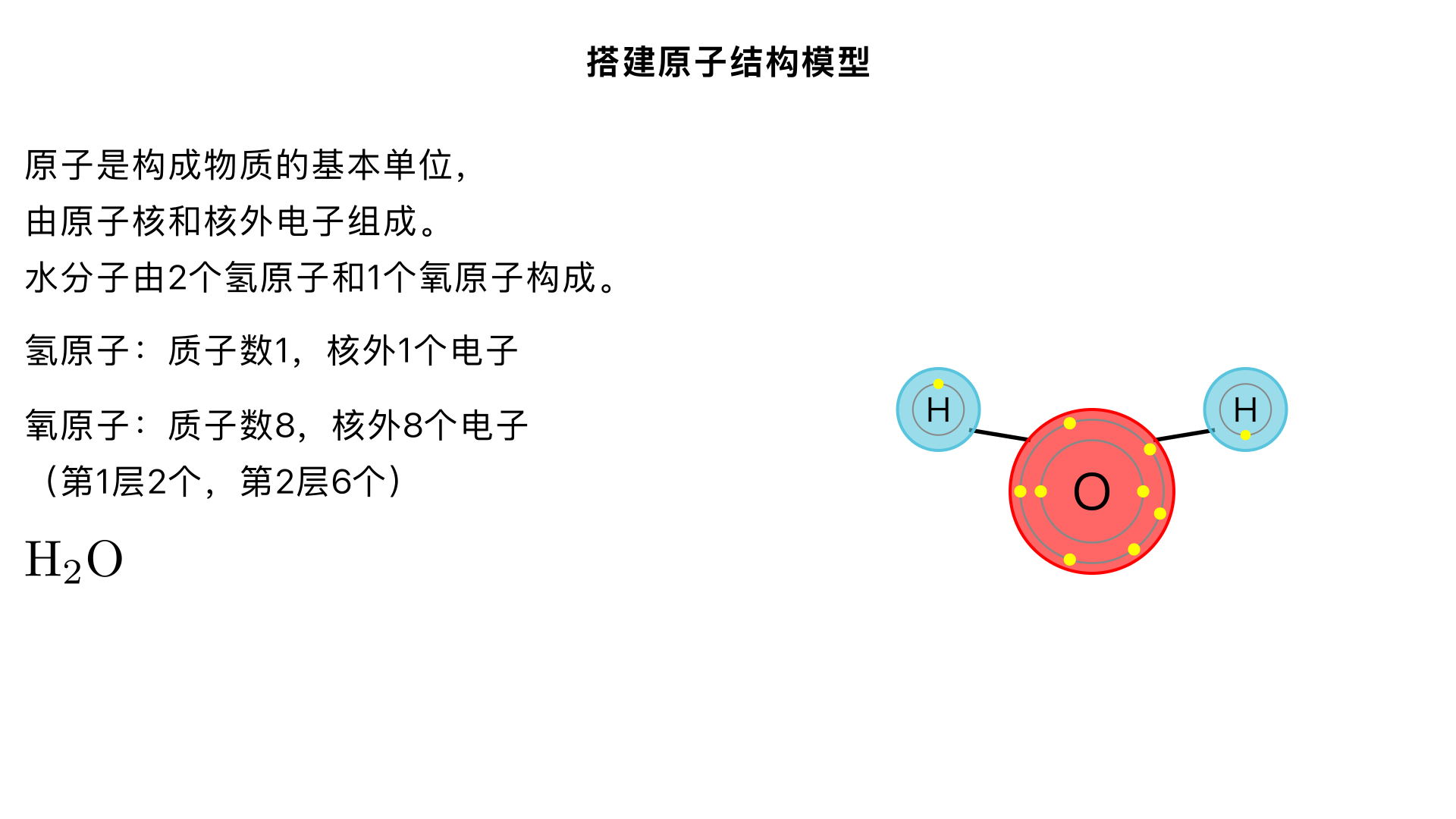
九年级化学 / 探究水的奥秘 / 搭建原子结构模型 本小节内容围绕原子结构基础和水分子的原子构成模型搭建展开,核心是帮助理解微观粒子的排布规律,以及水的微观构成本质,具体知识如下: 一、搭建原子结构模型的前提:原子的基本结构(九年级认知范畴) 原子的构成原子由原子核和核外电子构成,其中原子核又由质子和中子组成(普通氢原子无中子)。 质子:带 1 个单位正电荷,决定元素种类; 中子:不带电,影响原子的相对原子质量; 核外电子:带 1 个单位负电荷,分层排布,最外层电子数决定元素的化学性质。 九年级需掌握的氢、氧原子结构 氢原子:质子数为 1,核外只有 1 个电子,排布在第 1 层(最外层电子数为 1); 氧原子:质子数为 8,核外共 8 个电子,分 2 层排布(第 1 层 2 个,第 2 层 6 个,最外层电子数为 6)。 二、搭建水分子的原子结构模型(探究水的微观构成) 1. 模型搭建的依据 水的化学式为,表示 1 个水分子由2 个氢原子和1 个氧原子构成;从原子成键角度(九年级简化认知),氧原子最外层 6 个电子,需得到 2 个电子达到稳定结构,氢原子最外层 1 个电子,需得到 1 个电子达到稳定结构,因此 1 个氧原子会和 2 个氢原子通过共用电子对结合形成水分子。 2. 模型搭建的步骤(简易手工 / 示意图搭建) 准备材料:可选用不同颜色的小球(如红色代表氧原子、白色代表氢原子)、牙签(代表化学键);或用画图工具绘制模型。 定位中心原子:将代表氧原子的红色小球放在中心位置; 连接氢原子:用牙签将 2 个白色氢原子小球分别连接在氧原子两侧,形成 “V” 型结构(九年级阶段可简化为直线或 V 型,不深入空间构型细节); 标注粒子信息:在小球旁标注原子的质子数、核外电子层排布(可选),体现原子结构与成键的关联。 三、模型的意义与局限性 意义 直观呈现水的微观构成,建立 “宏观物质 - 微观粒子” 的联系; 帮助理解化学式的含义,为后续学习化学方程式奠定基础。 局限性 简易模型无法体现电子的动态运动和共用电子对的实际作用; 未展示原子内部的原子核结构,仅能体现原子层面的组合。 四、探究活动中的常见问题 误将水分子模型搭成直线型(实际为 V 型,九年级可说明是特殊的空间结构即可); 混淆原子和分子的界限,需强调 “模型中单个小球是原子,整体组合是分子”。
▶
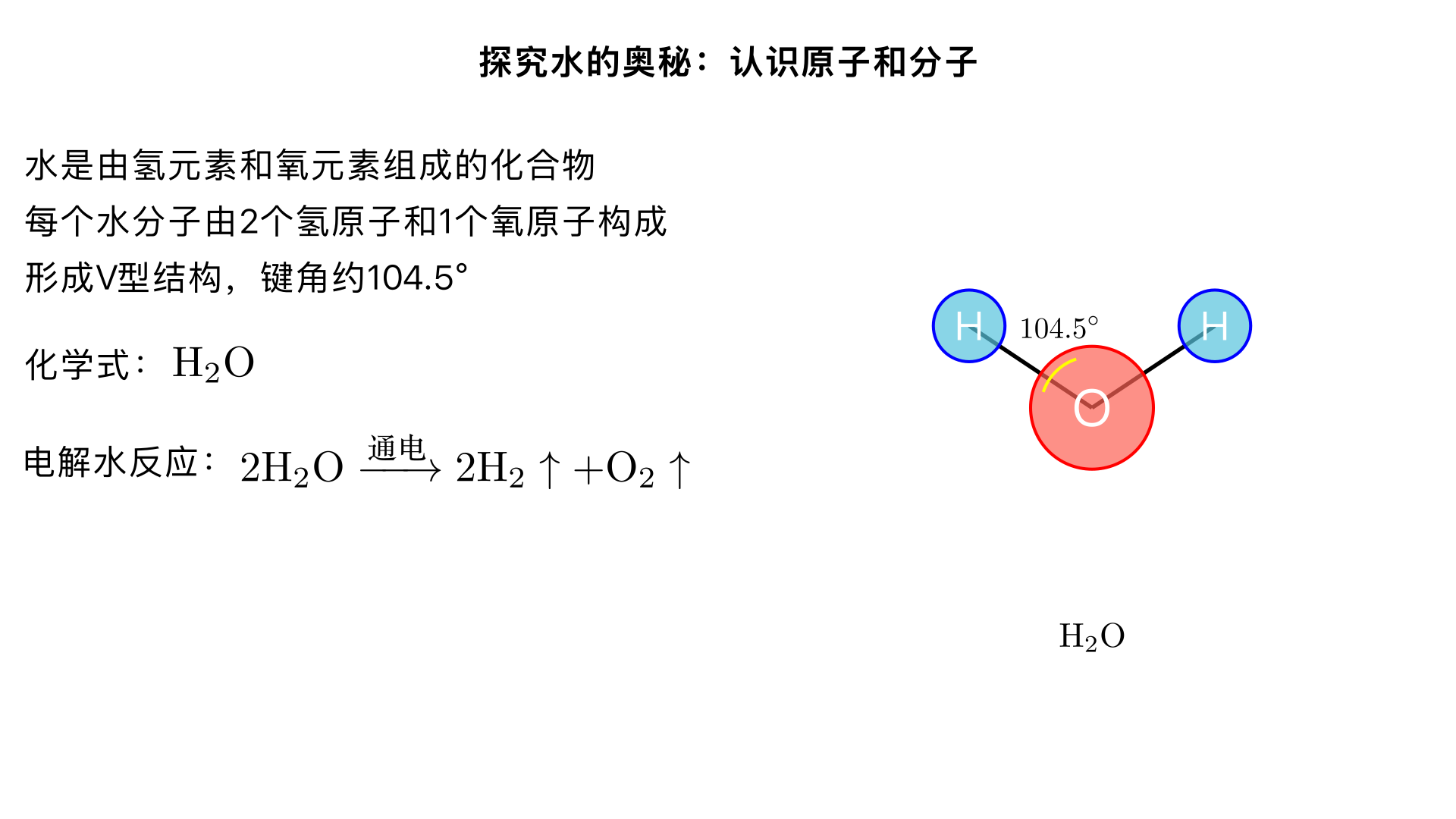
探究水的奥秘:认识原子和分子 一、物质的微观构成 1. 分子的概念 分子是保持物质化学性质的最小粒子(由分子构成的物质) 特点:质量和体积很小;不断运动(温度越高,运动越快);分子间有间隔(气体 > 液体 > 固体) 同种物质分子性质相同,不同物质分子性质不同 2. 原子的概念 原子是化学变化中的最小粒子,在化学反应中不可再分 分子由原子构成,如水分子由氢原子和氧原子构成 3. 分子与原子的区别 化学变化中:分子可分,原子不可分 分子是保持物质化学性质的最小粒子,原子是构成分子的基本单元 二、水的微观世界 1. 水的组成 水是由氢元素和氧元素组成的化合物,化学式为 H₂O 水由大量水分子构成,每个水分子由2 个氢原子和1 个氧原子通过共价键连接形成V 型结构 2. 水分子模型 氧原子位于中心,两个氢原子分别位于两侧,形成约 104.5° 的键角 水分子是极性分子,氧原子带部分负电荷,氢原子带部分正电荷,这导致水分子间形成氢键,赋予水独特的物理性质(如高沸点、高比热容) 三、探究活动:电解水实验 实验目的:验证水的组成,探究化学变化的微观本质 实验原理: plaintext 通电 2H₂O → 2H₂↑ + O₂↑ 实验装置与步骤: 准备霍夫曼电解器或简易电解装置(两个电极、电解液容器) 加入蒸馏水(或去离子水),并滴入少量硫酸钠或氢氧化钠以增强导电性 接通直流电源,观察电极上产生的气泡 记录两极气体体积:阴极 (负极) 产生氢气,阳极 (正极) 产生氧气,体积比约为2:1 微观解释: 通电时,水分子分裂成氢原子和氧原子(分子可分) 每 2 个氢原子结合成 1 个氢分子(H₂),大量氢分子聚集成氢气 每 2 个氧原子结合成 1 个氧分子(O₂),大量氧分子聚集成氧气 原子在反应前后种类不变、数目不变(原子不可分) 实验结论: 水由氢元素和氧元素组成 化学变化的实质是:分子分裂为原子,原子重新组合成新分子 四、活动:制作水分子模型 材料准备: 不同颜色的小球(或气球、橡皮泥):大球代表氧原子,小球代表氢原子 小木棍或吸管(代表化学键) 硬纸板(底座) 制作步骤: 取 1 个大球作为氧原子,2 个小球作为氢原子 将氧原子固定在底座中央 用木棍将两个氢原子连接到氧原子上,形成V 型结构(两氢原子夹角约 104.5°) 标注各原子名称及化学式 H₂O 拓展活动: 制作氢气分子(H₂)和氧气分子(O₂)模型,对比单质与化合物分子的区别 演示电解水的微观过程:将水分子模型拆开成原子,再重新组合成氢分子和氧分子,理解 "化学变化中分子可分,原子不可分" 的原理 五、用分子原子观点解释生活现象 1. 水的三态变化 固态 (冰)→液态 (水)→气态 (水蒸气):分子间间隔增大,分子运动加剧,但分子本身没有改变(物理变化) 2. 水的溶解能力 水分子的极性使它能溶解多种物质:极性分子(如糖)或离子化合物(如盐) 溶解过程:水分子包围溶质粒子,使其分散在水中 3. 为什么水结冰后体积膨胀? 液态水中水分子排列较紧密,结冰时形成规则的氢键网络,分子间空隙增大,导致体积膨胀,密度减小(冰浮于水) 六、总结提升 通过探究水的奥秘,我们认识到: 物质由微观粒子构成:分子、原子等 水分子:由 2 个氢原子和 1 个氧原子构成(H₂O),呈 V 型结构,是极性分子 化学变化的本质:分子分裂为原子,原子重新组合成新分子(原子守恒) 水的特性源于其独特的分子结构和分子间作用力(氢键) 思考与拓展: 查阅资料了解水的其他奇妙性质(如表面张力、毛细现象)与分子结构的关系 设计实验证明分子在不断运动(如浓氨水与酚酞的扩散实验) 思考:如果水分子结构不是 V 型而是直线型,水的性质会发生什么变化?

▶